克莱姆森大学的一组科学家正在了解体内通常产生的某些酶之间的关系以及它们在调节肥胖和控制肝脏疾病中的作用方面取得进展。
根据疾病控制和预防中心(CDC)在2017-18年收集的数据,超过42%的成年人和19%的年轻人肥胖。
来自埃默里大学医学院的三名克莱姆森研究人员及其同事研究了缺乏Cyp2b酶的雄性小鼠,以及缺乏酶如何影响小鼠的新陈代谢。
克莱姆森生物科学系教授兼研究生项目协调员威廉·鲍德温(William Baldwin)表示,这项研究部分是由一个简单的观察引发的:缺乏Cyp2b酶的雄性小鼠体重增加。在雌性Cyp2b-null小鼠中没有注意到相同的效果。
“我们注意到我们的Cyp2b-null小鼠更重,”生物科学系教授Baldwin说。“他们更容易肥胖 - 至少是饮食引起的肥胖 - 特别是在男性中,而不是野生型小鼠,我们试图找出为什么会这样。
虽然研究人员的观察结果非常简单,但事实证明,理解体重增加背后的相互作用要复杂得多。
“如果有一个很好,简单的答案,那就太好了,”鲍德温说,“但可能没有一个很好,简单的答案。
角色种类
Baldwin指出了涉及CYP酶的许多化学过程的复杂性,CYP酶是酶超家族的一部分,在人类中扮演着各种角色。他说,Cyp2b酶有助于代谢某些有毒物质和药物,以将它们从体内消除。
但这些相同的CYP酶也有其他工作。“它们代谢胆汁酸;它们代谢类固醇激素;它们从我们的饮食中代谢多不饱和脂肪,“鲍德温说。“这意味着所有这些东西也可以相互作用。如果你的饮食中充满了脂肪,这可能会抑制你的药物代谢。答案是肯定的。。。药物可能会抑制你的脂肪代谢,可能会影响你的类固醇代谢,等等。
研究人员还研究了“受干扰的脂质谱”与疾病之间的关联。
研究人员指出,疾病易感性和整体健康受到脂质组变化的极大影响。高脂肪饮食,如西方饮食,会导致肥胖并彻底改变肝脂质组,并且受干扰的脂质谱与特定的肝脏疾病有关,例如非酒精性脂肪性肝病(NAFLD)和非酒精性脂肪性肝炎(NASH)。
图片来源:克莱姆森大学
年龄和饮食的影响
鲍德温领导了之前对饮食和环境毒物之间关系的研究。最近的研究集中在年龄和饮食对这些代谢过程的影响上。
“不良饮食对我们有什么影响?年龄对我们有什么影响?这就是这里的想法,“鲍德温谈到最新的研究时说。“我们正在研究这些酶;随着时间的推移,与此小鼠模型中的配置文件相比,与野生型小鼠相比,会发生什么情况。随着时间的推移,高脂肪饮食可能会发生什么,随着年龄的增长,会发生什么,以及这种没有这些酶的小鼠模型与具有这些酶的小鼠模型之间的差异。
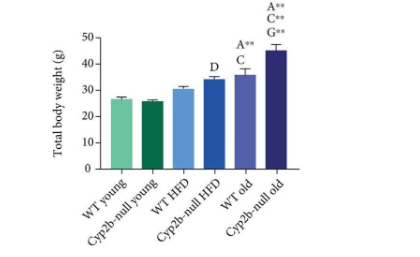
简单地说,鲍德温说,“我们看到的一件事,并不奇怪,就是变老是不好的。老鼠更难调节体重。他们体重增加。它们的重量是更多的白色脂肪组织[主要由脂肪细胞组成的结缔组织]。...其中一些事情在缺乏Cyp2b酶的小鼠中有点糟糕。它们有点重。他们的脂肪比同龄人多一点。他们的肝脏有点大,有点不健康。所以他们有很多与年龄有关的事情。
饮食也对老鼠的健康有影响。
“当然,饮食也没有帮助,”鲍德温继续说道。“情况也是如此:饮食不良会导致体重增加,而这些[Cyp2b-null]小鼠的情况更糟,可能是因为新陈代谢不良。
他说,Cyp2b酶工作的确切机制尚不完全清楚。
“你带走了一种有助于代谢这些的酶,但我认为它有助于摆脱脂肪并不重要,但它让身体知道脂肪在那里。它可能会产生信号分子,说,'嘿,我们需要决定我们要用这种脂肪做什么;我们需要分配这些脂肪。那种信息。这只是目前有根据的猜测,但我认为这可能就是正在发生的事情。
人类的差异
鲍德温说,他目前的研究仔细研究了正在发挥作用的机制,以及它们在人类模型中与小鼠研究的不同之处。他说,这项研究将成为尚未发表的论文的一部分,表明小鼠和人类酶的作用可能并不完全相同。“人类酶似乎导致我们在肝脏中保留一些脂肪,而小鼠酶似乎将其驱动到白色脂肪组织中。这篇论文中有一些暗示,情况就是这样,“鲍德温说。
该研究的结果发表在《脂质杂志》上,题为“雄性小鼠磷脂肝脏脂质组谱的年龄和饮食依赖性变化:Cyp2b-Null小鼠的年龄加速”。

