明尼苏达大学的研究人员和他们在国家癌症研究所(NCI)的合作者研究了一种新的细胞内检查点基因在调节T细胞功能对抗实体瘤中的作用。该团队被称为CISH,在Med上发表了结果,表明检查点基因在抑制人类T细胞识别和攻击癌细胞的能力方面发挥着关键作用。
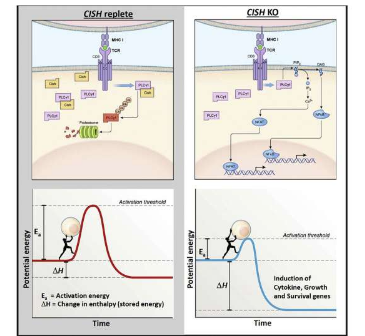
当CISH被禁用时,T细胞更有效地识别肿瘤产生的突变蛋白质。CISH抑制还保留了T细胞的适应性,并使T细胞对现有的检查点疗法更敏感,这为在癌症免疫疗法方面取得突破提供了一条新途径。
明尼苏达大学医学部助理教授BeauWebber博士说:“这是一个真实的临床案例,目前正被部署在已经用尽几乎所有其他治疗方案的转移性胃肠癌患者身上。”学校和共济会癌症中心的成员。“我们正在将实验室中的发现应用于寻求胃肠癌治疗的患者。”
由于CISH位于细胞内,因此不能像其他检查点分子被靶向一样使用抗体阻断剂来抑制它。为了克服这一挑战,由大学教员BrandenMoriarity博士和Webber博士领导的研究小组利用CRISPR基因编辑(一种切割DNA序列以删除和插入其他序列的过程)来安全有效地敲除CISH人类T细胞中的基因。这一过程有力地增强了T细胞识别和杀死肿瘤细胞的能力,并为明尼苏达大学使用CRISPR工程T细胞进行的首次人体临床试验奠定了临床前基础——这是唯一获得授权的第二次CRISPR临床试验。当时的食品药品监督管理局。
韦伯博士说:“这项工作是一项巨大的、多学科努力的成果,包括基本的机械免疫生物学、基因组编辑的尖端技术以及过继性细胞免疫疗法的最新进展。”
基因编辑提供了一种强大的新工具,使研究人员能够将检查点抑制硬连接到对抗肿瘤的特定免疫细胞中,从而加速新方法的临床转化。细胞内检查点基因,如CISH,特别令人感兴趣,因为它们提供了增强免疫细胞功能对抗癌症的新途径。
研究小组继续其正在进行的临床试验,并正在进行相关研究,以评估CISH编辑的肿瘤浸润淋巴细胞的功效和安全性。他们还在研究其他策略,以进一步改善工程免疫细胞对抗实体癌的功能。

